En juin 2021, l’Agence Nationale de Sécurité du Médicament et des Produits de Santé (ANSM) a été informée par la société Philips de sa volonté de retirer mondialement certains appareils de ventilation mécanique, suite à l’identification d’un possible problème de conception de la mousse insonorisante présente dans ses dispositifs médicaux.
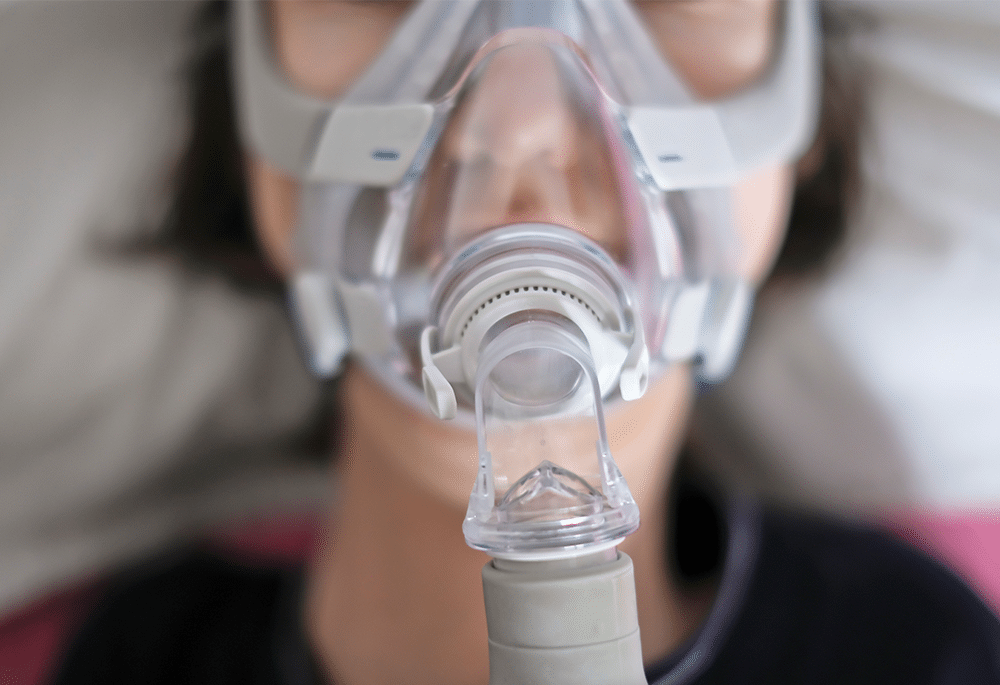
Les appareils concernés par cette alerte sont destinés aux personnes souffrant d’apnée du sommeil ou nécessitant une assistance respiratoire, utilisés principalement à domicile.
L’exposition à ces particules de mousse dégradée exposent les utilisateurs et utilisatrices à des risques potentiels comprenant des risques cancérigènes ainsi que des effets plus immédiats comme des irritations (peau, yeux et voies respiratoires), des réactions inflammatoires, des maux de tête, de l’asthme et des effets indésirables sur d’autres organes (par exemple, les reins et le foie).
Nous avons rapidement exprimé notre plus vive inquiétude concernant l’extrême lenteur des actions correctrices face au risque potentiellement cancérigène des dispositifs et devant la légitime angoisse de personnes contraintes de continuer à utiliser les appareils défectueux à défaut d’alternatives disponibles.
En février 2022, nous saluions la décision de police sanitaire prise par l’agence nationale de sécurité du médicament (ANSM) demandant notamment à la société Philips Respironics :
- D’accélérer son plan de remplacement avec deux échéances clés : 75 % de remplacement à fin juin 2022, 100% à fin décembre 2022
- De mettre en place une étude épidémiologique visant à objectiver le risque de cancer, les résultats préliminaires devant être transmis à l’ANSM dans un délai maximal d’un an
Les dernières échéances fixées par la décision de police sanitaire de l’ANSM sont terminées : où en est-on ?
Concernant le remplacement des appareils
A la fin décembre 2022, la société Philips a indiqué avoir procédé au remplacement de 98 % des appareils utilisés dans le traitement de l’apnée du sommeil. Cette estimation-qui mériterait d’être vérifiée-cache une douloureuse réalité.
A date, les ventilateurs utilisés en assistance respiratoire (Trilogy 100 et 200) n’ont fait l’objet d’aucun remplacement par Philips Respironics. Aucun plan de remplacement n’est prévu, ni transmis aux autorités. Cette situation, qui concerne de plus les personnes de loin les plus exposées aux risques, est inacceptable.
Concernant la mise en place d’une étude épidémiologique
Le 12 décembre dernier les représentants en France de la Société Philips précisaient avoir peu d’informations à ce stade.
La société Philips n’a donc pas répondu aux injections de l’autorité française :
- Des personnes continuent à utiliser ces ventilateurs faute de remplacement et ce 20 mois après le début de l’alerte
- Aucune étude complémentaire n’est fournie par Philips
France Assos Santé demande que toutes les injonctions de l’ANSM non respectées par Philips soient sanctionnées.
France Assos Santé réitère également sa demande auprès de l’ANSM de contraindre la société Philips au remplacement immédiat de l’ensemble des appareils défectueux y compris par le recours à des appareils d’autres fabricants non concernés par cette alerte sanitaire et ce par tous les moyens, y compris par voie judiciaire.
Nous estimons qu’il en va de la crédibilité de l’ANSM dans son rôle de police sanitaire.



Laisser un commentaire public