A la différence des médicaments, la réglementation relative aux dispositifs médicaux (traçabilité, classification, marquage) n’impose pas d’AMM (Autorisation de Mise sur le Marché). Après le scandale des prothèses mammaires PIP et le retrait de plusieurs dispositifs médicaux, le point sur les procédures de contrôle dont ils font l’objet.
L’appellation « dispositif médical » peut désigner un instrument, un appareil, un équipement ou un logiciel destiné, par son fabricant, à être utilisé chez l’homme. Objectifs des dispositifs médicaux : permettre le diagnostic, la prévention, le contrôle, le traitement et/ou l’atténuation d’une maladie ou d’une blessure. Sans dispositif médical, certaines procédures telles que le soin d’une fracture, le diagnostic du virus du SIDA ou l’implantation d’une prothèse seraient impossibles.
Classification des dispositifs médicaux et niveau de dangerosité
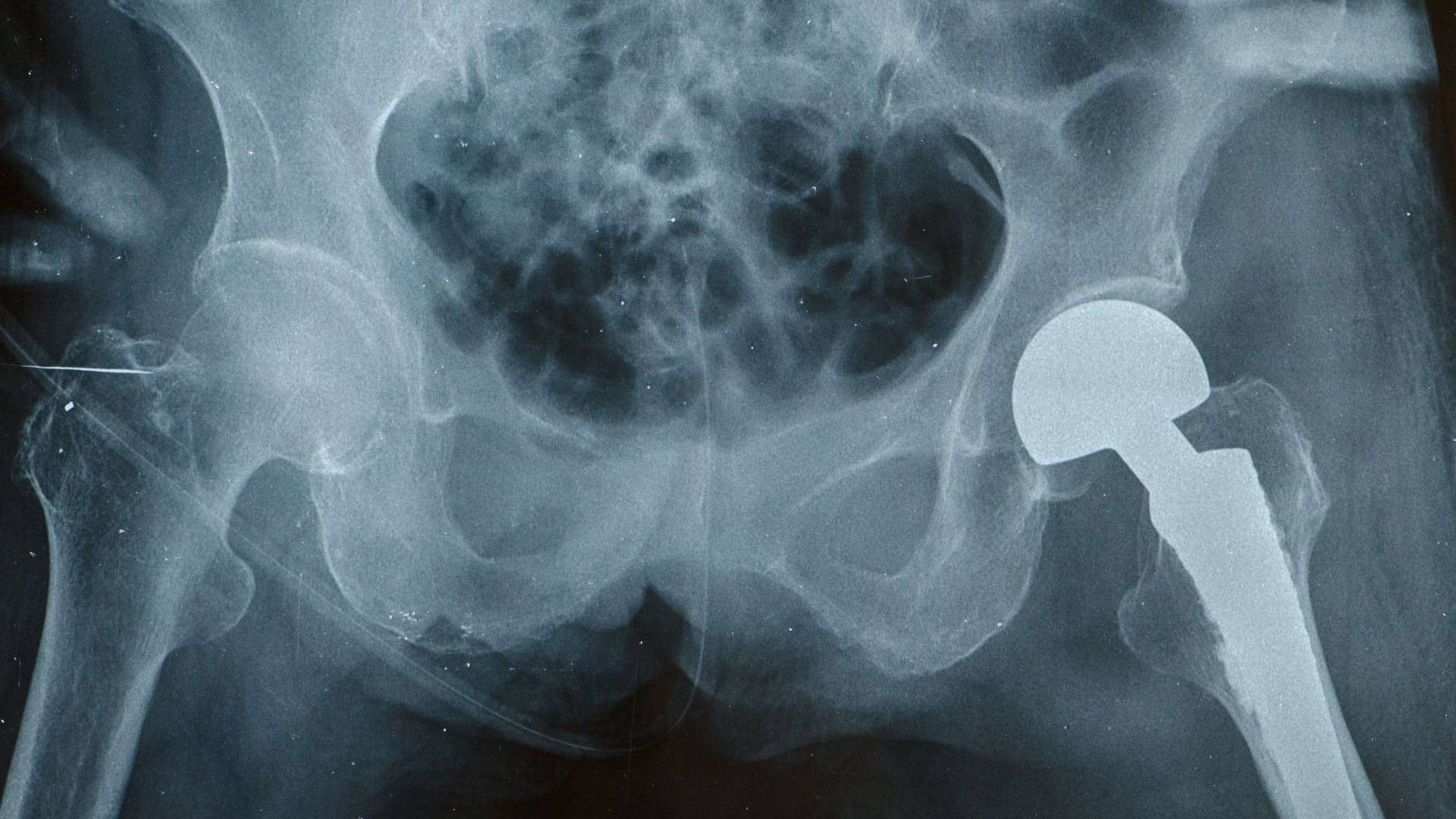
Béquille, paire de lunettes, prothèse de hanche, implant dentaire, préservatif, pansement… Les dispositifs médicaux (DM) s’avèrent particulièrement difficiles à caractériser en raison de leur extrême diversité !
Cette variété s’exprime à travers la nature même du dispositif médical, sa complexité, son application, son usage, ses utilisateurs et l’environnement dans lequel il est employé. A ce jour, l’Organisation mondiale de la Santé dénombre environ 10 000 catégories de dispositifs médicaux.
Au sein de cette classification, les produits situés à la frontière entre médicament et dispositif médical sont nombreux. A titre d’exemple, une seringue pré-remplie d’une substance médicamenteuse est considérée comme un médicament tandis que vide, elle devient un dispositif médical. D’une manière générale, qu’il s’agisse d’implants mammaires, de prothèses articulaires, de pansements, de fauteuils roulants… la classification des dispositifs médicaux se réfère à leur niveau de dangerosité.
Contrôle et marquage CE des dispositifs médicaux
Les dispositifs médicaux font l’objet d’un contrôle avant et après leur mise sur le marché. En amont, c’est le marquage CE qui garantit leur conformité pour une commercialisation en Europe. Ce marquage remplace l’autorisation de mise sur le marché qui permettrait de garantir l’efficacité, la sécurité et l’utilité des dispositifs médicaux.
Avec le marquage CE, c’est le fabricant du dispositif médical qui endosse la responsabilité de sa mise sur le marché. Ce marquage est le témoin de la conformité du dispositif médical aux exigences essentielles de santé et de sécurité fixées par les directives européennes.
C’est après la mise sur le marché d’un dispositif médical en France qu’intervient l’ANSM (Agence Nationale de Sécurité du Médicament et des Produits de Santé). Son rôle : surveiller le marché et vérifier la conformité des dispositifs médicaux.
Cette action comporte plusieurs volets :
- l’évaluation des incidents et les risques d’incidents que pourrait entraîner chaque dispositif médical. Bon à savoir : chaque citoyen peut signaler ce type d’informations sur l’espace dédié de l’ANSM,
- l’autorisation des investigations cliniques impliquant des dispositifs médicaux,
- l’habilitation des organismes chargés d’évaluer la conformité des dispositifs médicaux aux exigences essentielles,
- l’agrément des organismes chargés d’effectuer le contrôle de qualité auxquels sont soumis certains dispositifs médicaux.
Des règles de traçabilité spécifiques à certains dispositifs médicaux
Les dispositifs médicaux suivants bénéficient de règles de traçabilité particulières :
- les dispositifs médicaux incorporant une substance qui, si elle est utilisée séparément, est susceptible d’être considérée comme un médicament dérivé du sang,
- les valves cardiaques,
- les autres dispositifs médicaux implantables, y compris les implants dentaires, à l’exception des ligatures, sutures et dispositifs d’ostéosynthèse.
Ces règles de traçabilité permettent d’identifier les patients pour lesquels les dispositifs médicaux d’un lot particulier ont été utilisés. De la même manière, elles renseignent sur la provenance d’un dispositif médical utilisé chez un patient.
La loi sur la sécurité sanitaire des produits de santé du 29 décembre 2011 est venue notamment renforcer l’encadrement (marquage, classification, traçabilité) des dispositifs médicaux. Les règles de traçabilité ci-dessus énoncées vont dans ce sens. Elles pourraient permettre de se prémunir contre un nouveau scandale tel que celui des implants mammaires PIP. Mais ne faudrait-il pas redoubler de vigilance en amont et en aval de la commercialisation des dispositifs médicaux, voire réformer en profondeur le système d’évaluation de ces dispositifs ?
Traçabilité des dispositifs médicaux sur mesure : le cas des prothèses dentaires
La classification des prothèses dentaires respecte le statut de dispositif médical. Fabriquées sur mesure, ces prothèses nécessitent la prescription d’un chirurgien-dentiste qui précise les caractéristiques de conception pour chaque patient.
Comme la plupart des activités industrielles, la fabrication de ce type de dispositifs médicaux est soumise à la mondialisation. La réalisation d’une prothèse dentaire peut ainsi être sous-traitée à des opérateurs situés en dehors du territoire français. C’est alors le fabricant qui sous-traite tout ou partie de la production des dispositifs médicaux qui est responsable du produit fini. Il doit pouvoir justifier à tout moment du respect des réglementations et livrer des prothèses dentaires conformes aux exigences européennes en vigueur.
Ainsi, la documentation technique de la prothèse dentaire contient les informations sur les matériaux et les méthodes de fabrication de ce dispositif médical. Elle est établie par le fabricant et permet d’assurer notamment la traçabilité des produits auprès des autorités nationales, dont l’ANSM pour la France.
Des dispositions introduites en 2009 et 2010 améliorent la traçabilité de la chaîne de fabrication des dispositifs médicaux sur mesure et renforcent l’information délivrée aux personnes concernées par la pose d’une prothèse dentaire. Sur simple demande auprès de votre chirurgien-dentiste, il est dorénavant possible de disposer de la déclaration de conformité qui accompagne la prothèse dentaire. N’hésitez donc pas à la demander avant toute pose de prothèse.
Se documenter
- Voir le dossier de 66 Millions d’Impatients : Prothèses PIP – Les patientes au milieu du gué
- Décret n° 2006-1497 du 29 novembre 2006 et arrêté du 26 janvier 2007 relatifs aux règles particulières de matériovigilance exercée sur certains dispositifs médicaux.
- Liste des dispositifs médicaux sur le site de l’Ansm
- Bilan des règles applicables à la sécurité des dispositifs médicaux et propositions d’améliorations, dossier de l’Ansm, sept. 2012
- Parcours du dispositif médical, guide de la Haute Autorité de Santé
- L’Ansm a publié une fiche sur le bon usage des prothèses dentaires : Prothèse dentaire, ce que je dois savoir
- Loi n° 2009-879 du 21 juillet 2009 portant réforme de l’hôpital et relative aux patients, à la santé et aux territoires, qui étend l’obligation d’information écrite du patient à la charge du chirurgien-dentiste.



Bonjour,
En tant que patients, avons nous le droit d’accéder aux informations légales concernant un implant, comme la référence exacte, le fabricant, la classification, savoir si fabricant et distributeur satisfont aux bases de la réglementation?
Merci
Bonjour, pouvez vous me dire comment est libellé une prescription de prothèse dentaire, mon dentiste ne m’ en pas fait, de plus il ne m’a pas donné la fiche de traçabilité .
Merci pour votre réponse .